- Blog
13/01/2026
Pour décrire comment et dans quelles conditions vivent les souris de laboratoire, nous allons d’abord décrire une cage de souris, ensuite nous allons nous intéresser au macro puis au micro-environnement de ces animaux utilisés à des fins scientifiques.
Les souris de laboratoire vivent classiquement dans des cages en polycarbonate placées sur des portoirs à plusieurs étages (voir Figure 1). Les couvercles des cages peuvent être de simples grilles dans les animaleries dites conventionnelles, ou ces couvercles peuvent avoir des filtres très fins qui permettent de maintenir les souris dans des conditions propres grâce aux systèmes de portoirs ventilés (Individual Ventilated Cage : IVC) qui contrôlent l’air entrant et sortant (Hickman et al., 2017).
Une cage de souris aux dimensions standard a une surface au sol d’environ 500cm², avec une hauteur minimum de 12cm sur au moins 50% de la surface avec l’ajout des enrichissements (European parliament, 2010). Le nombre de souris pouvant être hébergées dans une cage dépend de leurs poids : il faut 60cm² par souris de 20g et 100cm² par souris de plus de 30g (European parliament, 2010). Les normes ont évolué entre les directives européennes de 1986 et 2010 puisque la surface minimale au sol indépendamment du nombre de souris par cage était de 180cm² dans la directive de 1986 et est maintenant de 330cm² avec la directive de 2010 (European Community Council, 1986; European parliament, 2010).

Le change de cage consiste à déplacer les souris d’une cage sale à une cage propre. La fréquence de ces changes varie selon les conditions d’hébergement et notamment en fonction de l’utilisation d’IVC ou non. La fréquence de change peut aller de deux fois par semaine à un change toutes les deux semaines voir plus (Hickman et al., 2017; Rosenbaum et al., 2009). Le choix de cette fréquence de change doit être basé sur deux éléments principaux :
Donc il faut changer les cages suffisamment régulièrement pour éviter qu’elles deviennent trop sales, mais par trop souvent pour limiter la fréquence du stress infligé au animaux.
A TransCure bioServices (TCS), pour maintenir le statut SOPF (Specific Opportunistic Pathogen Free) de nos souris, elles sont hébergées par groupes de 5 individus maximum par cage avec un système IVC. Le change a lieu toutes les deux semaines.
Les salles d’hébergement peuvent contenir plusieurs portoirs, chacun pouvant accueillir jusqu’à une centaine de cages. Une densité trop importante dans une salle d’hébergement peut engendrer des modifications des paramètres environnementaux et augmenter les échanges de phéromones (une souris stressée ou ayant subi une intervention douloureuse peut transmettre son angoisse aux souris hébergées dans sa cage ou à proximité) (Sterley et al., 2018).
Selon les directives de 1986 et 2010 (European Community Council, 1986; European parliament, 2010), les paramètres d’ambiance (température, humidité, cycle lumineux, ventilation et bruit) doivent être contrôlés. L’humidité doit être de 55% +/- 10% et la température entre 20 et 24°C (European Community Council, 1986), ces deux paramètres doivent être contrôlés quotidiennement. La ventilation et le bruit doivent faire l’objet d’un suivi régulier, il est important de limiter le bruit dans les salles d’hébergement puisqu’il peut avoir un impact important sur la santé et le bien-être des animaux. En 1986, la directive précise que l’utilisation d’un bruit de fond constant d’intensité modérée peut aider à masquer les bruits stressants (European Community Council, 1986; NC3Rs, 2021).
Dans la majorité des animaleries, surtout de statut sanitaire non conventionnel, l’éclairage est entièrement artificiel. La création d’une photopériode correspondant au cycle naturel des animaux est essentielle et obligatoire. Il est possible dans certains cas d’inverser le cycle lumière/obscurité afin de manipuler les souris, animaux nocturnes, durant leur phase d’éveil (voir Figure 2).
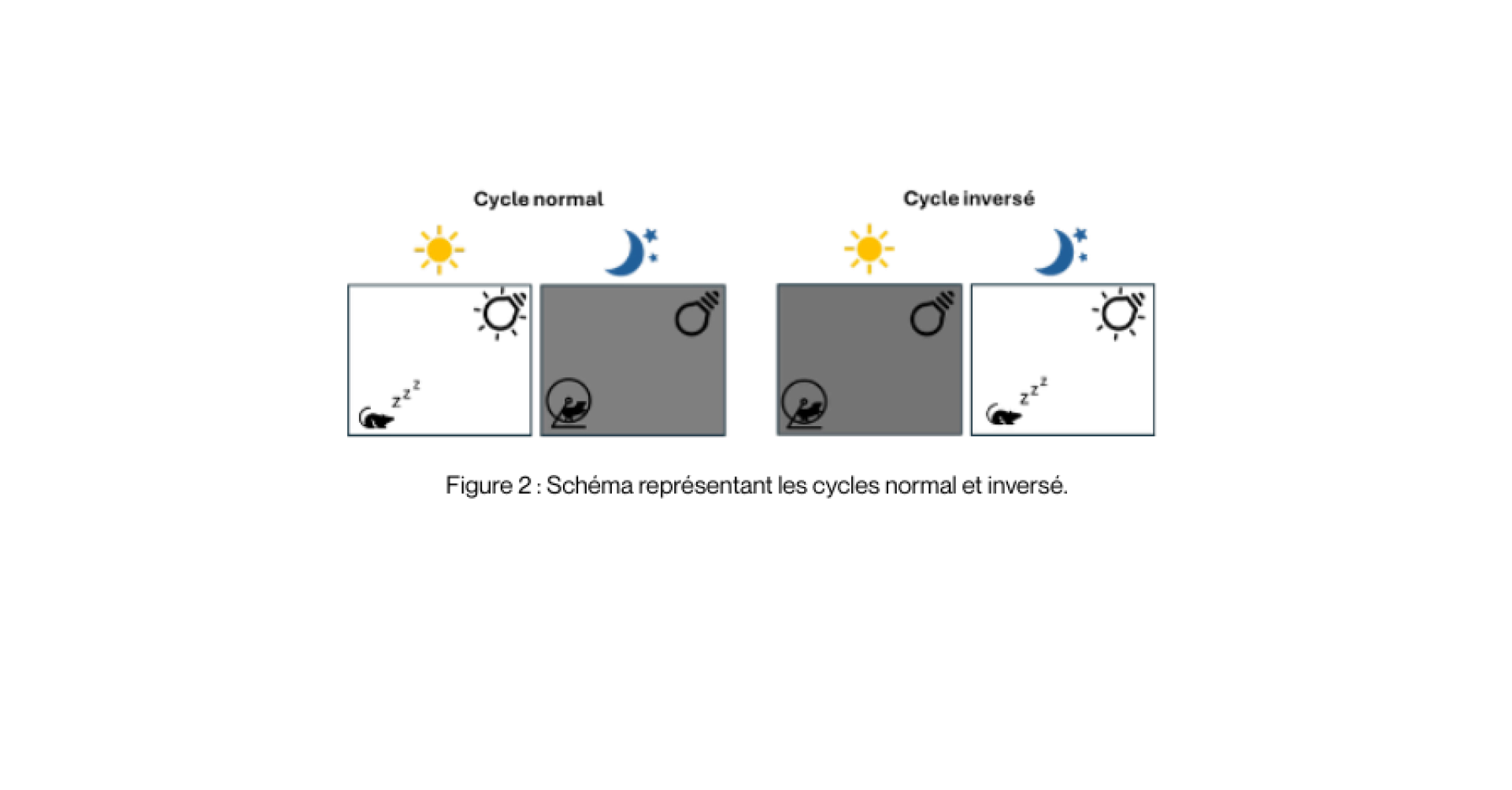
A TransCure bioServices, les souris sont hébergées en cycle normal de 12h/12h. Il est donc d’autant plus important de déranger au minimum les souris durant leur phase de sommeil. Le bruit est monitoré constamment et fait l’objet d’une attention particulière. Un bilan mensuel est réalisé et des mesures sont mises en place pour limiter au maximum les bruits notamment provenant du personnel travaillant dans l’animalerie. Chaque personne doit frapper aux portes avant d’entrer dans une salle d’hébergement afin d’éviter aux souris d’êtres surprises par un bruit soudain et un fond sonore est utilisé pour atténuer l’impact des bruits stressants.
Les éléments de base que doivent contenir une cage de souris sont de la nourriture, de l’eau (disponibles à volonté sauf si un protocole expérimental particulier exige une restriction) et de la litière. La nourriture des souris consiste en croquettes denses contenues dans des mangeoires. L’eau est disponible dans des biberons, des poches à eau ou via des dispositifs d’abreuvement automatiques. Il existe de très nombreuses litières différentes pouvant être utilisées dans les cages des souris, plus ou moins absorbantes et douces. En fonction de la litière et de la quantité utilisée, elle peut être considérée comme un enrichissement permettant aux souris de faire son nid et de pouvoir se reposer dans un endroit propre et sec (comme il est indiqué dans la directive de 2010).
Ces conditions standard d’hébergement sont pauvres et limitent l’expression des comportements propres aux souris. Les deux directives indiquent que les animaux devraient pouvoir exprimer le maximum de comportements propres à leur espèce. Ces directives n’obligent pas à ajouter des enrichissements mais l’encouragent. Lorsqu’elles en ont l’occasion, en captivité les souris font un nid, creusent, rongent, se cachent, grimpent, …. Elles ont également des comportements sociaux très développés et peuvent avoir des activités physiques et cognitives élaborées. Les enrichissements donnent l’opportunité aux animaux de réaliser tout ou partie de ces comportements.
Pour faire un nid, les souris ont besoin de matériaux structurants et doux qui leur permettent de construire une structure en 3 dimensions (voir Figure 3) qui peut les cacher complètement et augmenter la température au sein du nid (les souris ont une thermoneutralité d’environ 29°C) (Gordon, 2012; Kasza et al., 2023). Ces petits animaux sont tellement motivés pour réaliser ce comportement qu’il est utilisé pour mesurer notamment leur anxiété : lorsqu’une souris ne fait pas de nid ou le fait mal c’est un signe de mal-être (Deacon, 2006; Nollet, 2021). Des maisons en papier mâché ou en polycarbonate peuvent être ajoutées pour aider les souris à faire leur nid.

Le fait de creuser est un comportement difficile à reproduire de manière satisfaisante en captivité. C’est l’épaisseur de litière qui va surtout jouer sur la possibilité de réaliser plus ou moins ce comportement. L’Animal Research Review Panel conseille une épaisseur de litière d’au moins 2cm (Fawcett, 2012).
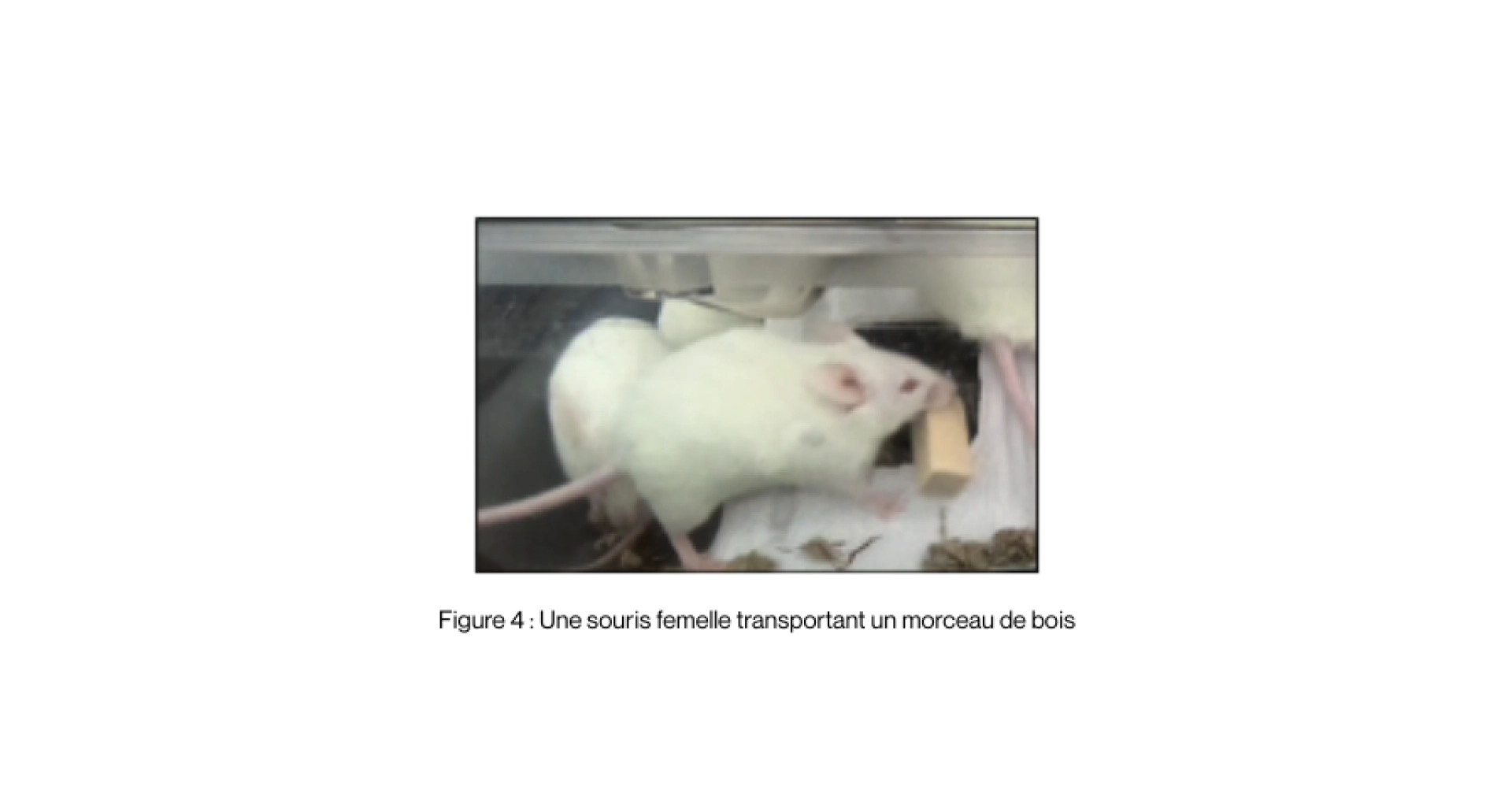
Le fait de ronger n’est pas seulement nécessaire pour le bien-être des souris, c’est également indispensable à leur santé puisque leurs dents poussent constamment et doivent être utilisées pour éviter des déformations pouvant empêcher les souris de manger (Brown & Donnelly, 2004). Les croquettes sont denses et permettent aux souris d’utiliser suffisamment leurs dents pour éviter les problèmes de santé. Des éléments supplémentaires comme des morceaux de bois peuvent être apportés pour séparer le comportement alimentaire de celui de ronger (voir Figure 4).
Les souris peuvent avoir besoin de se cacher de leurs congénères selon la hiérarchie installée au sein du groupe, mais aussi des potentiels prédateurs dont les humains. De nombreux enrichissements différents existent pour cela, de simples tunnels jusqu’à des constructions complexes. Ces enrichissements pour se cacher peuvent être en carton, en papier mâché ou encore en polycarbonate (ce qui permet de les réutiliser). Les formes sont diverses bien que les rongeurs en général apprécient particulièrement les tunnels (voir Figure 5).

Pour grimper, les souris ont généralement l’accès à la structure même de la cage. Si le couvercle est une grille elles peuvent se suspendre facilement à cette grille, si ce n’est pas le cas la mangeoire permet au moins d’avoir un accès à un élément pour grimper. D’autres enrichissements peuvent être ajoutés comme des cordes ou des échelles.
Les rongeurs sont très motivés à utiliser une roue lorsqu’elle est mise à leur disposition. Une souris ayant accès à volonté à une roue peut parcourir plusieurs kilomètres par jour (Zhu et al., 2020; Zhu et al., 2021) ! Plusieurs types de roues existent mais cet enrichissement prend beaucoup de place et ne peut pas systématiquement être utilisé dans l’espace restreint qu’est une cage. D’autres enrichissements cognitivo-moteurs peuvent être utilisés comme des hamacs par exemple.
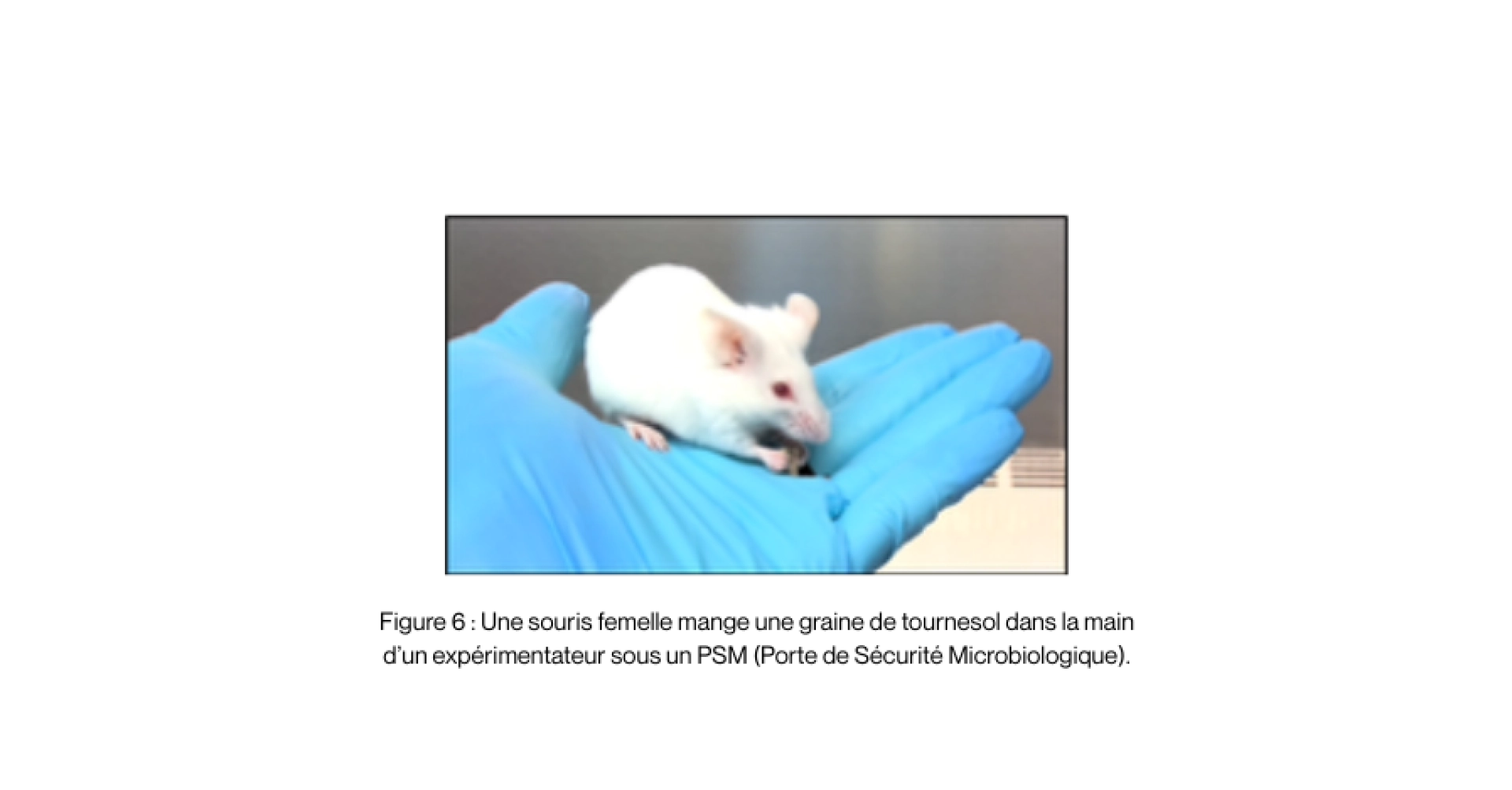
D’autres types d’enrichissement peuvent avoir plusieurs avantages. Par exemple, l’utilisation de graines de tournesol permet aux souris de réaliser plusieurs comportements qui leur sont propres comme fouiller dans la litière pour trouver la nourriture, utiliser la motricité fine pour ouvrir les graines, tenir la graine entre leurs pattes et la transporter entre leurs dents.

A TransCure bioServices, les souris ont accès à une litière particulièrement douce et à des fibres de papier kraft ce qui leur permet de creuser et de construire un nid chaud et bien structuré. Une petite maison et un tunnel sont utilisés pour que les souris se cachent ou dorment. En plus de croquettes, elles ont un morceau de bois par souris pour qu’elles puissent ronger et maintenir leurs dents en bonne santé. Des graines de tournesol sont utilisées comme friandises pour ces petits rongeurs qui les adorent (voir Figure 6).
Brown, C. J., & Donnelly, T. M. (2004). Rodent husbandry and care. In Veterinary Clinics of North America – Exotic Animal Practice (Vol. 7, Issue 2, pp. 201–225). W.B. Saunders. https://doi.org/10.1016/j.cvex.2004.02.005
Deacon, R. M. J. (2006). Assessing nest building in mice. Nature Protocols, 1(3), 1117–1119. https://doi.org/10.1038/nprot.2006.170
European Community Council. (1986). Directive 86/609/CEE.
European parliament and of the council of 22 September 2010 on the protection of animals used for scientific purposes. (2010). Directive 2010/63/EU.
Fawcett, A. (2012). Guidelines for the Housing of Mice in Scientific Institutions.
Gordon, C. J. (2012). Thermal physiology of laboratory mice: Defining thermoneutrality. Journal of Thermal Biology, 37(8), 654–685. https://doi.org/10.1016/J.JTHERBIO.2012.08.004
Hickman, D., Hickman-Davis, J., Peveler, J., & Swan, M. (2017). Small Animal Enclosures and Housing. In Management of animal care and use programs in research, education, and testing (pp. 479–505).
Kasza, I., Cuncannan, C., Michaud, J., Nelson, D., Yen, C. L. E., Jain, R., Simcox, J., MacDougald, O. A., Parks, B. W., & Alexander, C. M. (2023). “Humanizing” mouse environments: Humidity, diurnal cycles and thermoneutrality. Biochimie, 210, 82–98. https://doi.org/10.1016/j.biochi.2022.10.015
NC3Rs. (2021). Housing and husbandry: Mouse.
Nollet, M. (2021). Models of Depression: Unpredictable Chronic Mild Stress in Mice. Current Protocols, 1(8). https://doi.org/10.1002/cpz1.208
Rosenbaum, M. D., VandeWoude, S., & Johnson, T. E. (2009). Effects of Cage-Change Frequency and Bedding Volume on Mice and Their Microenvironment. Journal of the American Association for Laboratory Animal Science, 48(6), 763–773.
Sterley, T. L., Baimoukhametova, D., Füzesi, T., Zurek, A. A., Daviu, N., Rasiah, N. P., Rosenegger, D., & Bains, J. S. (2018). Social transmission and buffering of synaptic changes after stress. Nature Neuroscience, 21(3), 393–403. https://doi.org/10.1038/s41593-017-0044-6
Washington, I. M., & Payton, M. E. (2016). Ammonia Levels and Urine-Spot Characteristics as Cage-Change Indicators for High-Density Individually Ventilated Mouse Cages. Journal of the American Association for Laboratory Animal Science, 55(3), 260–267.
Zhu, J. lian, Luo, W. wen, Cheng, X., Li, Y., Zhang, Q. zhi, & Peng, W. xing. (2020). Vitamin D deficiency and Schizophrenia in Adults: A Systematic Review and Meta-analysis of Observational Studies. Psychiatry Research, 288(April). https://doi.org/10.1016/j.psychres.2020.112959
Zhu, M., Kasaragod, D. K., Kikutani, K., Taguchi, K., & Aizawa, H. (2021). A novel microcontroller-based system for the wheel-running activity in mice. ENeuro, 8(6). https://doi.org/10.1523/ENEURO.0260-21.2021