- Actualités
20/01/2026

Les scientifiques ont longtemps essayé de reproduire la procédure qui a conduit à la première rémission à long terme du patient « Berliner », il y a 12 ans. Hier, ils semblent avoir réussi avec le patient « London » qui s’est libéré du VIH après une greffe de cellules souches de la moelle osseuse.
Cette nouvelle est porteuse de beaucoup d’espoir pour les patients infectés par le VIH ! Nous sommes fiers de pouvoir contribuer à de telles percées en fournissant aux chercheurs du monde entier des modèles murins appropriés de la maladie du VIH pour l’évaluation de traitements et de schémas thérapeutiques anti-VIH plus efficaces.
Lire l’article complet ci-dessous :
4 mars 2019
Pour la deuxième fois depuis le début de l’épidémie mondiale, un patient semble avoir été guéri de l’infection par le V.I.H., le virus qui cause le sida.
Cette nouvelle intervient près de 12 ans jour pour jour après la guérison du premier patient connu, un exploit que les chercheurs ont longtemps tenté, sans succès, de reproduire. Ce succès surprise confirme qu’il est possible de guérir l’infection par le V.I.H., même si c’est difficile, ont déclaré les chercheurs.
Les chercheurs publieront leur rapport mardi dans la revue Nature et présenteront certains détails lors de la conférence sur les rétrovirus et les infections opportunistes qui se tiendra à Seattle.
Publiquement, les scientifiques décrivent le cas comme une rémission à long terme. Lors des interviews, la plupart des experts parlent de guérison, tout en précisant qu’il est difficile de définir ce terme lorsqu’il n’existe que deux cas connus.
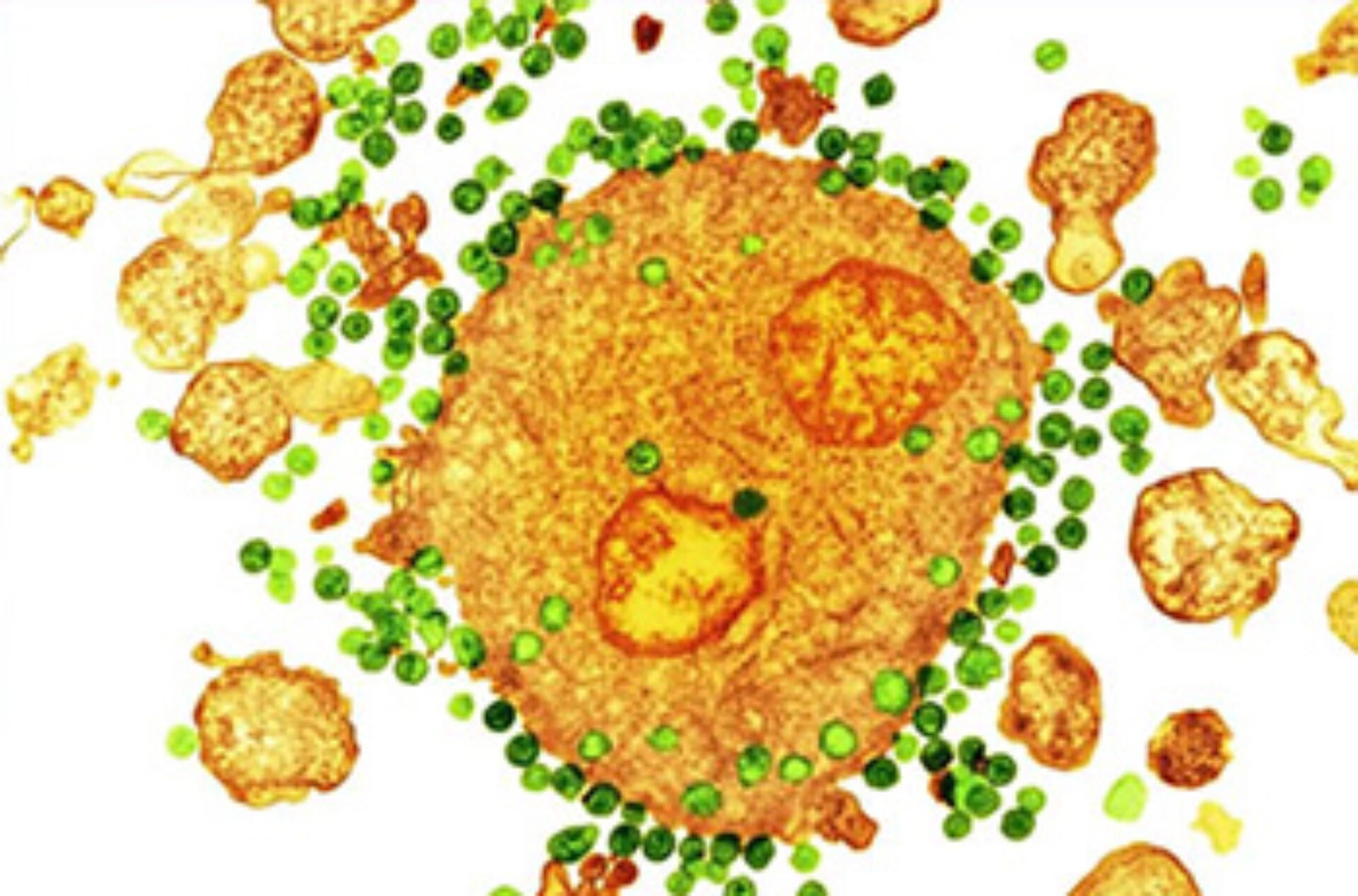
Micrographie électronique à transmission colorée du virus H.I.V., en vert, s’attachant à un globule blanc, en orange. Crédit : NIBSC/Science Source.
Ces deux étapes ont été franchies grâce à des greffes de moelle osseuse effectuées sur des patients infectés. Mais ces greffes étaient destinées à traiter le cancer des patients, et non le V.I.H.
Il est peu probable que la greffe de moelle osseuse soit une option thérapeutique réaliste dans un avenir proche. Des médicaments puissants sont aujourd’hui disponibles pour contrôler l’infection par le V.I.H., tandis que les greffes sont risquées, avec des effets secondaires graves qui peuvent durer des années.
Mais réarmer le corps avec des cellules immunitaires modifiées de la même manière pour résister au V.I.H. pourrait bien réussir en tant que traitement pratique, selon les experts.
« Annemarie Wensing, virologue au centre médical universitaire d’Utrecht, aux Pays-Bas, a déclaré : »Cela inspirera les gens en leur montrant que la guérison n’est pas un rêve. « C’est à portée de main.
Le Dr Wensing codirige IciStem, un consortium de scientifiques européens qui étudient les greffes de cellules souches pour traiter l’infection par le V.I.H. Le consortium est soutenu par AMFAR, une organisation américaine de recherche sur le SIDA. Le consortium est soutenu par AMFAR, l’organisation américaine de recherche sur le sida.
Le nouveau patient a choisi de rester anonyme et les scientifiques ne l’ont appelé que « le patient de Londres ».
« Je me sens responsable d’aider les médecins à comprendre comment cela s’est produit afin qu’ils puissent développer la science », a-t-il déclaré au New York Times dans un courriel.
Apprendre qu’il pouvait être guéri à la fois du cancer et de l’infection par le V.I.H. a été « surréaliste » et « bouleversant », a-t-il ajouté. « Je n’aurais jamais pensé qu’il y aurait un remède de mon vivant.
Lors de la même conférence en 2007, un médecin allemand a décrit la première guérison de ce type chez le « patient de Berlin », identifié plus tard comme Timothy Ray Brown, 52 ans, qui vit aujourd’hui à Palm Springs, en Californie.
Cette nouvelle, affichée sur un poster au fond d’une salle de conférence, n’a d’abord guère attiré l’attention. Lorsqu’il est devenu évident que M. Brown était guéri, les scientifiques ont entrepris de reproduire ce résultat avec d’autres patients cancéreux infectés par le V.I.H.
. Dans tous les cas, le virus est réapparu, souvent environ neuf mois après que les patients ont cessé de prendre des médicaments antirétroviraux, ou bien les patients sont décédés du cancer. Ces échecs ont amené les scientifiques à se demander si la guérison de M. Brown resterait un coup de chance.
M. Brown a souffert d’une leucémie et, la chimiothérapie n’ayant pas réussi à l’enrayer, il a dû subir deux greffes de moelle osseuse.
Ces greffes provenaient d’un donneur présentant une mutation d’une protéine appelée CCR5, qui se trouve à la surface de certaines cellules immunitaires. Le V.I.H. utilise cette protéine pour pénétrer dans ces cellules, mais ne peut pas s’accrocher à la version mutée.
M. Brown a reçu des médicaments immunosuppresseurs puissants, d’un type qui n’est plus utilisé, et a souffert de graves complications pendant des mois après la transplantation. À un moment donné, il a été plongé dans un coma artificiel et a failli mourir.

Timothy Ray Brown, la première personne à avoir été guérie du V.I.H., a failli mourir pendant le traitement.Credit : Grant Hindsley for The New York Times
« Il a vraiment été battu par toute la procédure », a déclaré le Dr Steven Deeks, un expert du SIDA à l’Université de Californie, San Francisco, qui a traité M. Brown. « Nous nous sommes toujours demandé si ce conditionnement, cette destruction massive de son système immunitaire, n’expliquait pas pourquoi Timothy était guéri et personne d’autre.
Le patient londonien a répondu à cette question : Il n’est pas nécessaire d’avoir frôlé la mort pour que la procédure fonctionne.
Atteint d’un lymphome de Hodgkin, il a reçu une greffe de moelle osseuse d’un donneur porteur de la mutation CCR5 en mai 2016. Il a également reçu des médicaments immunosuppresseurs, mais le traitement était beaucoup moins intense, conformément aux normes actuelles pour les patients transplantés.
Il a cessé de prendre des médicaments anti-VIH en septembre 2017, ce qui fait de lui le premier patient connu depuis M. Brown à rester sans virus pendant plus d’un an après l’arrêt du traitement.
« Je pense que cela change un peu la donne », a déclaré le Dr Ravindra Gupta, virologue à l’University College London, qui a présenté les résultats lors de la réunion de Seattle. « Tout le monde croyait, après le patient de Berlin, qu’il fallait pratiquement mourir pour guérir du V.I.H., mais aujourd’hui, ce n’est peut-être pas le cas.
Bien que le patient londonien n’ait pas été aussi malade que M. Brown après la transplantation, la procédure a fonctionné à peu près aussi bien : La greffe a détruit le cancer sans effets secondaires nocifs. Les cellules immunitaires transplantées, désormais résistantes au V.I.H., semblent avoir entièrement remplacé ses cellules vulnérables.
La plupart des personnes porteuses de la mutation résistante au V.I.H., appelée delta 32, sont originaires d’Europe du Nord. IciStem dispose d’une base de données d’environ 22 000 donneurs de ce type.
À ce jour, ses scientifiques suivent 38 personnes infectées par le V.I.H. qui ont reçu une greffe de moelle osseuse, dont six provenant de donneurs ne présentant pas la mutation.
Le patient de Londres figure au 36e rang de cette liste. Un autre patient, numéro 19 sur la liste et appelé « patient de Düsseldorf », n’a pas pris de médicaments anti-VIH depuis quatre mois. Les détails de ce cas seront présentés à la conférence de Seattle dans le courant de la semaine.
Les scientifiques du consortium ont analysé à plusieurs reprises le sang du patient de Londres à la recherche de signes du virus. Ils ont constaté une faible indication de la poursuite de l’infection dans l’un des 24 tests, mais affirment que cela pourrait résulter d’une contamination de l’échantillon.
Le test le plus sensible n’a pas révélé de virus en circulation. Des anticorps contre le VHI étaient toujours présents dans son sang, mais leurs niveaux ont diminué avec le temps, selon une trajectoire similaire à celle observée chez M. Brown.
Rien ne garantit que le patient londonien soit définitivement tiré d’affaire, mais les similitudes avec la guérison de M. Brown incitent à l’optimisme, a déclaré le Dr Gupta.
« D’une certaine manière, la seule personne avec laquelle on peut faire une comparaison directe est le patient de Berlin. « C’est en quelque sorte la seule norme dont nous disposons pour le moment.
« Je pense que cela change un peu la donne », a déclaré le Dr Ravindra Gupta, virologue à l’University College de Londres. Crédit : Jane Stockdale pour le New York Times
La plupart des experts qui connaissent les détails s’accordent à dire que le nouveau cas semble être un remède légitime, mais certains doutent de sa pertinence pour le traitement du sida en général.
« Je ne suis pas sûr de ce que cela nous apprend », a déclaré le Dr Anthony Fauci, directeur de l’Institut national des allergies et des maladies infectieuses. « Cela a été fait avec Timothy Ray Brown, et maintenant il y a un autre cas – ok, et maintenant quoi ? Qu’allons-nous faire maintenant ? »
Une possibilité, selon le Dr Deeks et d’autres, est de développer des approches de thérapie génique pour éliminer le CCR5 des cellules immunitaires ou de leurs prédécesseurs, les cellules souches. Résistantes à l’infection par le V.I.H., ces cellules modifiées devraient à terme débarrasser l’organisme du virus.
(Le CCR5 est la protéine que He Jiankui, un scientifique chinois, a prétendu avoir modifiée par édition génétique chez au moins deux enfants, dans le but de les rendre résistants au V.I.H. – une expérience qui a suscité une condamnation internationale).
Plusieurs entreprises s’intéressent aux thérapies géniques, mais n’ont pas encore réussi. La modification doit cibler le bon nombre de cellules, au bon endroit – uniquement la moelle osseuse, par exemple, et non le cerveau – et ne modifier que les gènes qui dirigent la production de CCR5.
« Il y a un certain nombre de niveaux de précision à atteindre », a déclaré le Dr Mike McCune, conseiller principal en matière de santé mondiale auprès de la Fondation Bill et Melinda Gates. « On peut également craindre qu’il se produise quelque chose de fâcheux et, dans ce cas, on peut souhaiter disposer d’un interrupteur d’arrêt.
Plusieurs équipes travaillent sur tous ces obstacles, a déclaré le Dr McCune. À terme, elles pourraient être en mesure de mettre au point un système d’administration virale qui, une fois injecté dans le corps, recherche tous les récepteurs CCR5 et les supprime, ou même une cellule souche de donneur qui résiste au V.I.H. mais qui pourrait être administrée à n’importe quel patient.
« Ce sont des rêves, n’est-ce pas ? Des choses sur la table à dessin », a déclaré le Dr McCune. « Ces rêves sont motivés par des cas comme celui-ci – ils nous aident à imaginer ce qui pourrait être fait à l’avenir.
Une mise en garde importante concernant une telle approche est que le patient resterait vulnérable à une forme de V.I.H. appelée X4, qui utilise une protéine différente, CXCR4, pour pénétrer dans les cellules.
« Cela ne fonctionnera que si le virus n’utilise que la protéine CCR5 pour pénétrer dans les cellules, ce qui est le cas d’environ 50 % des personnes vivant avec le V.I.H., voire moins », a déclaré le Dr Timothy J. Henrich, spécialiste du sida à l’université de Californie à San Francisco.
Même si une personne n’héberge qu’un petit nombre de virus X4, ceux-ci peuvent se multiplier en l’absence de concurrence de leurs cousins viraux. Il existe au moins un cas rapporté d’une personne ayant reçu une greffe d’un donneur delta 32, mais qui a ensuite rebondi avec le virus X4. (Par mesure de précaution contre le X4, M. Brown prend une pilule quotidienne pour prévenir l’infection par le V.I.H.).
M. Brown espère que la guérison du patient londonien sera aussi durable que la sienne. « Si quelque chose s’est produit une fois dans la science médicale, cela peut se reproduire », a déclaré M. Brown. « J’attends la compagnie depuis longtemps.
Un gâteau offert à M. Brown pour marquer les 12 ans de sa guérison, lors d’un atelier à la bibliothèque publique de Seattle, dimanche. Crédit : Grant Hindsley pour le New York Times